IPA Journal 01/2024
Staubproben an Arbeitsplätzen untersuchen, Endotoxine messen
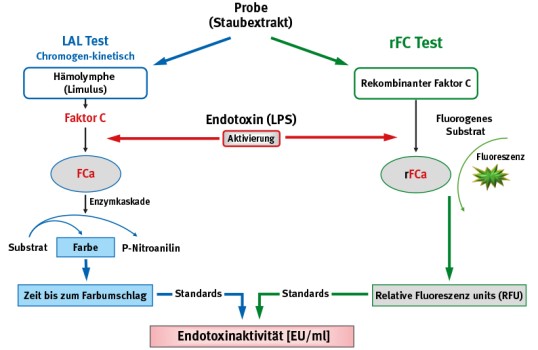
Abb. 1: Der Nachweis von Endotoxin erfolgt über seine Fähigkeit, Enzyme zu aktivieren. Diese Enzymaktivität wird im LAL-Test in einer mehrstufigen Reaktionskaskade gemessen, die letztlich zu einem Farbumschlag der Proben führt. Die Zeit bis zum Farbumschlag unterscheidet sich je nach Konzentration. Auch im rFC-Test wird die Endotoxinaktivität gemessen, allerdings wird hier statt Zeit Fluoreszenz gemessen.
Qualitätsprüfung der Messverfahren
Staub am Arbeitsplatz, sei es in der Industrie, Landwirtschaft oder auch im Büro, kann gesundheitlich belastend sein. Entscheidend für das Gefährdungspotential des Staubes ist neben der Zusammensetzung vor allem die Dosis. Um diese Wirkfaktoren zu ermitteln, bedarf es valider Messverfahren. Eine wichtige Forschungsaufgabe ist es deshalb, die Qualität der Messmethoden zu überprüfen und sie auf dem wissenschaftlich aktuellen Stand zu halten.
Pilze, Bakterien oder Viren, spricht man von Bioaerosolen. Ihre Zusammensetzung kann je nach Arbeitsplatz stark variieren. Allerdings können Bioaersosole beim Einatmen sowie bei Haut- oder Augenkontakt, infektiös, entzündlich oder allergisierend wirken. Je nach Art des Bioaerosols, Dauer und Intensität des Kontakts und persönlicher Empfindlichkeit kann sich die gesundheitliche Wirkung unterscheiden. Der Aufwand, alle Komponenten solcher luftgetragenen Stäube zu untersuchen, ist immens. Deswegen konzentriert man sich meist auf die Analyse einzelner Leitkomponenten, wie den Endotoxinen (Liebers et al. 2007). Dabei handelt es sich um Bestandteile der äußeren Zellmembran von Gram-negativen Bakterien oder Cyanobakterien (→ Info), die bei deren Absterben freigesetzt werden. Endotoxine kommen nahezu überall vor. Sie können bei entsprechend hoher Exposition an staubigen Arbeitsplätzen gesundheitliche Beschwerden verursachen (Liebers et al. 2006 und 2020). Chemisch betrachtet sind Endotoxine Lipopolysaccharide, die aus einem Vielfachzucker (Polysaccharid) und einem Lipidanteil bestehen und hitzestabil sind.
Tests zum Nachweis von Endotoxinen
Der Nachweis von Endotoxinen erfolgt über ihre Fähigkeit, Enzyme zu aktivieren. Dafür hat sich bisher in vielen Laboren der sogenannte Limulus-Amöbozyten-Lysat (LAL)-Test etabliert.
Der Pfeilschwanzkrebs (Limulus) besitzt statt Blut als zirkulierende Körperflüssigkeit die sogenannte Hämolymphe. Sie gerinnt, sobald das Enzym Serinprotease aktiviert wird. Die Aktivierung des Enzyms kann durch Endotoxine erfolgen. Dieser Mechanismus ist die Basis für das ursprüngliche Testverfahren, den LAL-Test. Mit Hilfe der gerinnenden Hämolymphe wurden drei Varianten des LAL-Tests entwickelt, wobei der chromogen-kinetische LAL-Test die überwiegend genutzte Methode darstellt, um Endotoxin in Arbeitsplatzproben oder aus der Umwelt zu analysieren. Chromogen-kinetisch bedeutet, dass ein Farbumschlag im Zeitverlauf gemessen wird.
Um einerseits auf tierisches Material zu verzichten und andererseits den Test besser zu standardisieren, haben verschiedene Hersteller mittels rekombinant – künstlich mit Hilfe von gentechnisch veränderten Mikroorganismen – hergestellter Enzyme alternative Messsysteme aufgebaut. So auch den rFC-Test (= rekombinanter Faktor C Test). Bei ihm wurde allerdings nicht nur das Enzym, die Serinprotease Faktor C, im Reagenzglas hergestellt, sondern auch das Messprinzip verändert. Statt anhand einer mehrstufigen Aktivierungskaskade mit Farbreaktion, erfolgt die Messung über einen einstufigen Fluoreszensassay (Liebers et al. 2019a, 2019b) (Abb. 1).
Aufgrund der Vorteile des neuen Testsystems ist es sinnvoll, den rFC-Test für zukünftige Studien zu etablieren. Jedoch erfordert jede Umstellung von einem bereits etablierten System wie dem LAL-Test auf ein neues Verfahrens eine Validierung des neuen Testsystems. So soll geklärt werden, ob die neue Methode den Anforderungen an Spezifität und Sensitivität gerecht wird (→ Info), und inwieweit sie mit der ursprünglichen Methode vergleichbar ist.
Die wissenschaftliche Prüfung von Verfahren ist auch wichtig, um abzuschätzen, welche Parameter Messergebnisse beeinflussen können.
Für die vorliegende Studie wurden elektrostatische Staubsammler (electrostatic dust sampler = EDC) eingesetzt (Liebers et al. 2023). Hiermit können sowohl Allergene als auch Endotoxine über einen längeren Zeitraum mit geringem Personalaufwand gesammelt werden (Sander et al. 2023; Zahradnik et al. 2022).
Vergleichsuntersuchung am IPA mit Staubextrakten
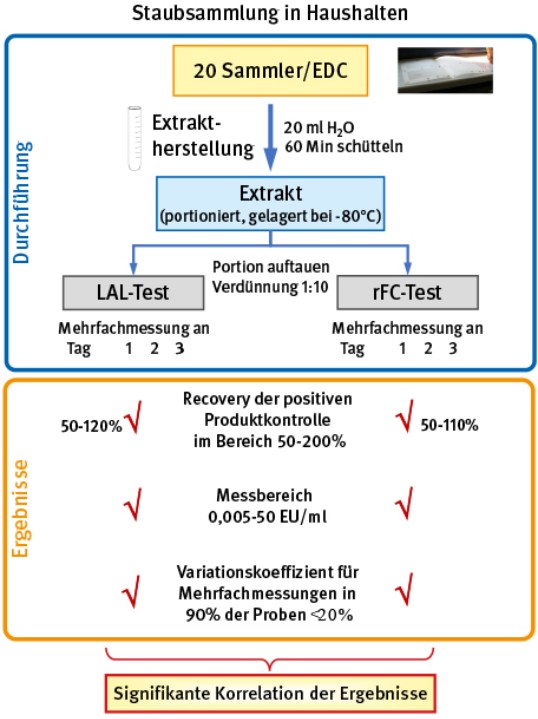
Insgesamt wurden von 20 EDCs, auf denen sich für 14 Tage Luftstaub abgesetzt hatte, wässrige Extrakte hergestellt. Diese wurden zunächst portioniert und anschließend bei -80 C eingefroren. Nach dem Auftauen und vor den Messungen wurden sie für maximal drei Tage im Kühlschrank aufbewahrt (Abb. 2, 3).
Um die Reproduzierbarkeit der Messungen zu überprüfen, erfolgte der Vergleich von Mehrfachmessungen, sowohl im LAL- als auch im rFC-Test. Zusätzlich wurde die Reproduzierbarkeit der zugehörigen Standardkurven geprüft.
Prüfung der Standardkurven, Mehrfachmessungen und der Einsatz von positiven Produktkontrollen dienen insgesamt der Qualitätsüberprüfung.
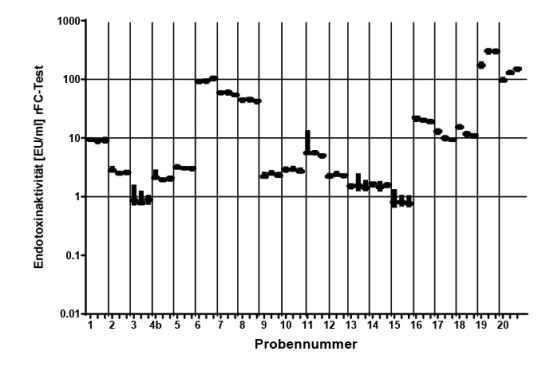
Endotoxinaktivität von 20 Staubextrakten, gemessen im rFC-Test. Jede Probe wurde 8fach an drei aufeinanderfolgenden Tagen gemessen. Die Balken zeigen Minimum und Maximum dieser Bestimmungen. Die schwarzen Linien markieren orientierende Kategorien von <1/<10/<100 oder >100 EU/ml in dieser logarithmischen Darstellung.
1. Standardkurven
Zu jeder Endotoxinmessung gehört eine Standardreihe mit definierten Endotoxinkonzentrationen von 0 bis 50 Endotoxin-Units (EU/ml). Zwölf unabhängige Standardkurven kamen in dieser Studie für jeweils LAL- als auch rFC-Test zum Einsatz. Der Variationskoeffizient der Doppelbestimmungen lag im Median über alle Konzentrationen bei 9 % für den rFC-Test und 12 % für den LAL-Test.
2. Mehrfachmessungen
An drei aufeinander folgenden Tagen wurden die 20 Probenextrakte parallel sieben beziehungsweise acht Mal gemessen. Nach dem Auftauen lagerten die Proben im Kühlschrank. Diesem Versuchsansatz lag die Überlegung zugrunde, dass in der Praxis Staubextrakte innerhalb eines Zeitraums von drei Tagen gemessen werden, ohne erneut eingefroren zu sein. Bei 90 % der Proben unterschieden sich die Mehrfachbestimmungen um weniger als 20 % und lagen damit in einem für Messungen von biologischem Material akzeptablen Bereich (Abb. 3).
3. Produktkontrollen: Endotoxinaktivität in der Probe wiederfinden
Die Probenzusammensetzung, aber auch Lagerung und Verarbeitung kann zu Störungen bei der Aktivitätsbestimmung der Endotoxine führen. Deshalb wird empfohlen, jede Probe in einem zweiten Ansatz mit definiert zugefügtem Endotoxin zu messen. Dieses Kontroll-Endotoxin muss sich bei der Messung in einem gewissen Rahmen wiederfinden lassen. Man spricht hier von der sogenannten Wiederfindungsrate, auch Recovery genannt. Ist das nicht der Fall, weist das auf eine Über- oder Unterschätzung der Messwerte hin. Solche Störungen lassen sich im Regelfall durch das Verdünnen der Probe beseitigen.
Entsprechend der Herstellerangabe und der Pharmakopöe (→ Info), genügt es, wenn diese positive Produktkontrolle zwischen 50 und 200 % liegt, um grobe Fehleinschätzungen zu vermeiden. In den Untersuchungen am IPA wurde ein Zusatz von 5 EU/ml als positive Produktkontrolle verwendet. Die Recovery für die 20 untersuchten Proben lag beim rFC-Test im Median bei 94 % und bei 69 % für den LAL-Test. Zwei Proben, die in der ersten Messung Recovery-Werte unter 50 % aufwiesen, konnten in höherer Verdünnung korrekt analysiert werden. Damit waren alle eingesetzten Proben analysierbar.
Ausblick
Die Mehrfachmessungen zeigten, dass sowohl LAL als auch rFC -Test gut reproduzierbare Ergebnisse liefern, sofern derselbe, zuvor eingefrorene Staubextrakt wiederholt eingesetzt wird. Für die Untersuchung von Bioaerosolen ist aber zu bedenken, dass Art und Ort der Sammlung die Zusammensetzung und den Anteil von Endotoxin verändern. Daher bedarf es einer zusammenfassenden Bewertung, um die jeweilige Exposition an Arbeitsplätzen korrekt zu beschreiben. Mit LAL- und rFC-Test stehen geeignete Verfahren zur Verfügung, um Endotoxine aus Staubextrakten anhand ihrer Aktivität valide zu bestimmen. Um Tierversuche zu vermeiden und auch die Reproduzierbarkeit einzelner Testchargen zu erhöhen, sind rekombinante Verfahren gegenüber dem ursprünglichen LAL-Test zu bevorzugen.
Kurz gefasst
Stäube an Arbeitsplätzen, die Partikel biologischer Herkunft enthalten, können infektiös, entzündlich oder allergisierend wirken.
Um mögliche gesundheitsschädliche Wirkungen zu identifizieren, bedarf es valider Messverfahren.
Am IPA wurde die Neueinführung einer Endotoxin-Messmethode überprüft.
Autorinnen

Dr. Verena Liebers
Maria Düser
Prof. Dr. Monika Raulf
IPA
Info

Gram-negativ: Durch ein Färbeverfahren (Gramfärbung) lassen sich Gram-negative von Gram-positiven Bakterien unterscheiden. Die unterschiedliche Färbung entsteht, weil diese Bakteriengruppen sich hinsichtlich ihrer Zellwand unterscheiden. Nur Gram-negative Bakterien besitzen in der äußeren Zellmembran Verbindungen aus Fett (Lipo-) und Zucker-Bestandteilen (Polysacchariden). Diese Lipopolysaccharide, wirken beim Zerfallen der Bakterien als Endotoxine.
Pharmakopoe: Arzneibuch, Sammlung anerkannter pharmazeutischer Regeln
Spezifität/Sensitivität: Spezifität beschreibt die Genauigkeit, Sensitivität die Empfindlichkeit, mit der ein Verfahren die gesuchte Substanz misst.
Literatur

Liebers V, Brüning T, Raulf-Heimsoth M. Occupational endotoxin-exposure and possible health effects on humans. Am J Ind Med 2006; 49: 474-91
Liebers V, Brüning T, Raulf M. Occupational endotoxin exposure and health effects. Arch Toxicol 2020; 94: 3629-3644
Liebers V, Düser M, Kendzia B, Brüning T, Raulf, M. Quantifizierung von Endotoxin mit dem rekombinanten Faktor-V-(rFC)-Test – Vergleich mit dem LAL-Test. Gefahrstoffe Reinhaltung der Luft 2019a; 79: 337-341
Liebers V, Gärtner A, Düser M, Kendzia B, Brüning T, Raulf M. Quantification of endotoxin activity with recombinant Factor C assay – method for avoiding animal experiments. Umwelt – Hygiene – Arbeitsmed 2019b; 24: 427-428
Liebers V, Raulf-Heimsoth M, Linsel G, Goldscheid N, Düser M, Stubel H, Brüning T. Evaluation of quantification methods of occupational endotoxin exposure. J Toxicol Environ Health A 2007; 70: 1798-805
Liebers V, van Kampen V, Bünger J, Düser M, Stubel H, Brüning T, Raulf-Heimsoth M. Assessment of airborne exposure to endotoxin and pyrogenic active dust using electrostatic dustfall collectors (EDCs). J Toxicol Environ Health A 2012; 75: 501-7
Liebers V, Düser M, Raulf M. Quality control of endotoxin measurement in dust samples. Gefahrstoffe Reinhaltung der Luft 2023; 10: 203-208
Sander I, Lotz A, Liebers V, Zahradnik E, Sauke-Gensow U, Petersen J, Raulf M. Comparing the concentration levels of allergens and endotoxins in employees‘ homes and offices. Int Arch Occup Environ Health 2022; 95: 573-588
Zahradnik E, Sander I, Kleinmüller O, Lotz A, Liebers V, Janssen-Weets B, Kler S, Hilger C, Beine A, Hoffmeyer F, Nienhaus A, Raulf M. Animal Allergens, Endotoxin, and b-(1,3)-Glucan in Small Animal Practices: Exposure Levels at Work and in Homes of Veterinary Staff. Ann Work Expo Health 2022; 66: 27-40